أنواع التفاعلات الشائعة للمحفزات المعدنية الثمينة المتجانسة
مقدمة
يشيع استخدام المعادن الثمينة مثل البلاتين والبلاديوم والروديوم والذهب كمحفزات متجانسة نظرًا لنشاطها التحفيزي العالي وانتقائيتها وثباتها. كما أنها معروفة أيضًا بثباتها الحراري الكبير وخمولها الكيميائي، مما يجعلها محفزات استثنائية. وبفضل هذه الخصائص، تجد محفزات الفلزات الثمينة المتجانسة مجموعة واسعة من التطبيقات، مثل المستحضرات الصيدلانية والبتروكيماويات والكيماويات وعلوم المواد.
سنتحدث في هذه المقالة عن أنواع التفاعلات الشائعة للمحفزات الفلزية الثمينة المتجانسة. نأمل أن يكون لديك مزيد من الفهم لهذه المحفزات القيمة.

الشكل 1. محفزات المعادن الثمينة
أنواع التفاعلات الشائعة لمحفزات الفلزات الثمينة المتجانسة
تُستخدم محفزات المعادن الثمينة المتجانسة في مجموعة متنوعة من التفاعلات. ومن الأمثلة النموذجية على ذلك الهدرجة وتفاعلات الهيدروجين والهيدروفورميلية وتفاعلات الاقتران وما إلى ذلك.
--الهيدروجين:
الهدرجة هي تفاعل يتم فيه إضافة الهيدروجين إلى مركبات عضوية غير مشبعة، وعادةً ما يتم ذلك بمساعدة عامل حفاز. تُستخدم المحفزات المتجانسة مثل البلاتين والبلاديوم على نطاق واسع في تفاعلات الهدرجة لتحويل الألكينات إلى ألكانات ومركبات النيترو إلى أمينات.

الشكل 2. تفاعلات الهدرجة ونزع الهيدروجين المحفزة بالفلزات لتخزين الهيدروجين بكفاءة [1]
--نزع الهيدروجين:
نزع الهيدروجين هو عكس الهدرجة التي يتم فيها إزالة الهيدروجين من الجزيء. تُستخدم محفزات المعادن الثمينة مثل البلاتين والروديوم في تفاعلات نزع الهيدروجين لصنع الألكينات من الألكانات ومركبات الكربونيل من الكحوليات.
--الأكسدة:
في تفاعلات الأكسدة، يفقد الجزيء إلكترونات، وتُستخدم محفزات الفلزات الثمينة المتجانسة لتحويل الكحولات إلى ألدهيدات أو كيتونات، والألكينات إلى إيبوكسيدات. ومن بين تفاعلات الأكسدة هذه، تُعد عملية "هوكست-واكر" أشهرها، حيث يتم تصنيع الأسيتالديهيد من الإيثين والأكسجين باستخدام محفزات Pd/Cu في محاليل مائية تحتوي على الكلوريد.
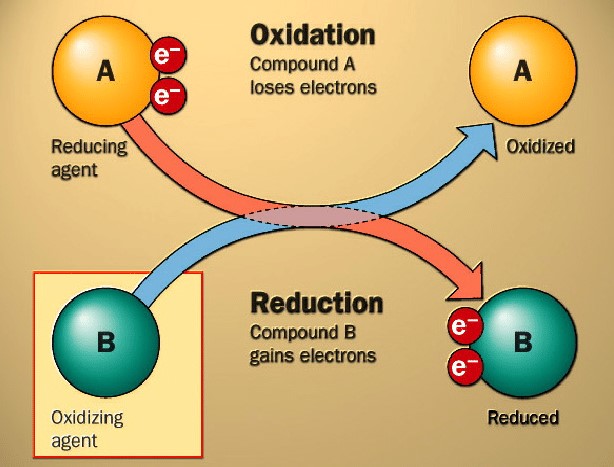
الشكل 3. الأكسدة والاختزال الأساسيان [2]
--الاختزال
الاختزال هو عكس الأكسدة، حيث يكتسب الجزيء إلكترونات. تُستخدم هذه العوامل الحفازة المتجانسة بشكل عام في تفاعلات الاختزال لتحويل مركبات النيترو إلى أمينات ومركبات الكربونيل إلى كحوليات.
-الاقتران:
تنطوي تفاعلات الاقتران على ربط جزيئين أو أكثر لتكوين جزيء أكبر. يتم استخدام البلاديوم والبلاتين والعوامل الحفازة الأخرى في تفاعلات الاقتران لتكوين روابط كربون-كربون، كما هو الحال في تفاعل سوزوكي وتفاعل هيك.
--الكربنة
تشير الكربنة إلى التفاعلات التي تشكل الألدهيدات والكيتونات وما إلى ذلك باستخدام أول أكسيد الكربون (CO). العملية الأكثر شهرة هي كربنة الميثانول إلى حمض الأسيتيك. وتسمى أيضًا عملية مونسانتو. ولا يمكن تحقيق جميع هذه العمليات بدون محفزات الروديوم.
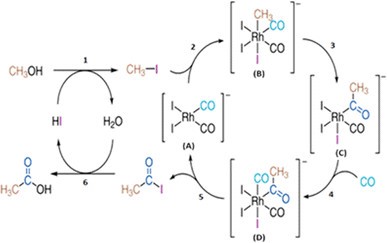
الشكل 4. الدورات التحفيزية المقترحة لتفاعل كربنة الميثانول المحفّز بالروديوم (عملية مونسانتو) [3]
-الهيدروفورميلية:
تُعرف الهيدروفورميلية أيضًا باسم تخليق الأكسو. تحول هذه العملية الألكينات إلى ألدهيدات بمزيج من أول أكسيد الكربون (CO) والهيدروجين (H2). حلت محفزات الروديوم محل محفز الكوبالت السابق في مثل هذه العمليات.
--الأيزومرة:
الأيزومرة هو تفاعل يخضع فيه الجزيء لإعادة ترتيب بنيوي. ويُعد البلاتين والروديوم من المحفزات المتجانسة النموذجية المستخدمة في تفاعلات الأيزومرة لتحويل الألكانات إلى ألكانات متفرعة والألكينات إلى أيزومرات.
يمكنك الاطلاع على الجدول أدناه لمعرفة المزيد عن المقارنة بين أنواع التفاعلات المختلفة للعوامل الحفازة المتجانسة للمعادن الثمينة المتجانسة.
الجدول 1. أنواع التفاعلات المختلفة لمحفزات الفلزات الثمينة المتجانسة
|
|
التعريف |
أمثلة |
|
الهدرجة |
إضافة الهيدروجين |
تحويل الألكينات إلى ألكانات، ومركبات النيترو إلى أمينات; |
|
نزع الهيدروجين |
إزالة الهيدروجين; |
تحويل الألكانات إلى ألكانات، والكحولات إلى مركبات الكربونيل; |
|
الأكسدة |
فقدان الانتخابات |
تحويل الكحوليات إلى ألدهيدات أو كيتونات، والألكينات إلى إيبوكسيدات |
|
الاختزال |
اكتساب الإلكترونات |
تحويل مركبات النيترو إلى أمينات، ومركبات الكربونيل إلى كحوليات; |
|
الاقتران |
اقتران جزيئين أو أكثر لتكوين جزيء أكبر; |
تفاعل سوزوكي وتفاعل هيك; |
|
الكربنة |
تكوين الألدهيدات والكيتونات باستخدام أول أكسيد الكربون (CO); |
عملية مونسانتو |
|
الهيدروفورميلية |
تحويل الألكينات إلى ألدهيدات باستخدام أول أكسيد الكربون (CO) والهيدروجين (H2); |
استخدام محفزات الروديوم |
|
الأيزومرة |
الترتيبات الهيكلية; |
تحويل الألكانات إلى ألكانات متفرعة، والألكينات إلى أيزومرات; |
الخاتمة
باختصار، تُستخدم محفزات الفلزات الثمينة المتجانسة على نطاق واسع في مختلف التفاعلات الكيميائية، بما في ذلك الهدرجة ونزع الهيدروجين والأكسدة والاختزال والاقتران والكربنة والهيدروفورميلية والأيزومرة. إن نشاطها التحفيزي العالي وانتقائيتها وثباتها يجعلها أدوات لا تقدر بثمن للكيميائيين في الصناعات الدوائية والبتروكيماوية والصناعات الكيميائية الدقيقة. ومن خلال فهم أنواع التفاعلات الشائعة للمحفزات المعدنية الثمينة المتجانسة، يمكن للعلماء تطوير عمليات كيميائية أكثر كفاءة واستدامة.
تُعد Stanford Advanced Materials (SAM) موردًا موثوقًا للمحفزات البلاتينية ومحفزات البلاديوم وغيرها من محفزات المعادن الثمينة . أرسل لنا استفسارًا إذا كنت مهتمًا.
المرجع:
[1] شيمباياشي، تاكويا وفوجيتا، كين-إيتشي. (2020). تفاعلات الهدرجة المحفزة للمعادن ونزع الهيدروجين لتخزين الهيدروجين بكفاءة. تيتراهيدرون. 76. 130946. 10.1016/j.tet.2020.130946.
[2] أزمان، نور ورملي، محمد وعيسى، سيتي. (2019). مراجعة تهجين الأنابيب النانوية الكربونية في الجرافين لتطبيق مستشعر الغاز. سلسلة مؤتمرات IOP: علوم وهندسة المواد. 551. 012017. 10.1088/1757-899X/551/1/012017.
[3] Budiman, Anatta & Nam, Ji & Park, Jae & Mukti, Mukti, Ryan & Chang, Tae & Bae, Jong Wook & Choi, Myoung. (2016). مراجعة تخليق حمض الخليك من مختلف المواد الأولية من خلال عمليات تحفيزية مختلفة. مسوحات الحفز من آسيا. 20. 10.1007/s10563-016-9215-9.

 القضبان
القضبان
 الخرز والكرات
الخرز والكرات
 البراغي والصواميل
البراغي والصواميل
 البوتقات
البوتقات
 الأقراص
الأقراص
 الألياف والأقمشة
الألياف والأقمشة
 الأفلام
الأفلام
 فليك
فليك
 الرغاوي
الرغاوي
 رقائق معدنية
رقائق معدنية
 الحبيبات
الحبيبات
 أقراص العسل
أقراص العسل
 الحبر
الحبر
 صفائح
صفائح
 الكتل
الكتل
 التشابك
التشابك
 غشاء معدني
غشاء معدني
 اللوحة
اللوحة
 المساحيق
المساحيق
 قضيب
قضيب
 الصفائح
الصفائح
 البلورات المفردة
البلورات المفردة
 هدف الاخرق
هدف الاخرق
 الأنابيب
الأنابيب
 الغسالة
الغسالة
 الأسلاك
الأسلاك
 المحولات والآلات الحاسبة
المحولات والآلات الحاسبة



 Chin Trento
Chin Trento



